Nell'approvvigionamento idrico industriale e nel trattamento delle acque reflue, l'addolcimento con scambio ionico è una delle tecnologie di controllo della qualità dell'acqua più classiche e ampiamente utilizzate. Sebbene "scambio di resina" sia un termine familiare agli ingegneri, l'equilibrio ionico sottostante e i meccanismi di reazione reversibili determinano direttamente l'effetto di ammorbidimento, la durata della resina e l'economia della rigenerazione. Con l'emergere di nuovi processi come le acque reflue ad alta-salinità e i sistemi a-scarico zero, i principi tradizionali dello scambio ionico si trovano ad affrontare nuove sfide-perché l'efficienza dell'addolcimento diminuisce in modo significativo nell'acqua ad alta-salinità? Perché la concentrazione della salamoia di rigenerazione deve essere controllata al 6%–10%? Questo articolo inizierà con l'equilibrio chimico dello scambio ionico, analizzando in modo approfondito le leggi di reazione essenziali delle resine a scambio cationico durante la trasformazione, l'addolcimento e la rigenerazione, fornendo basi teoriche e indicazioni pratiche per gli ingegneri per ottimizzare i parametri operativi del sistema.
I. Principi di base dello scambio ionico e della rigenerazione
I processi di trasformazione, rammollimento e rigenerazione delle resine a scambio cationico sono essenzialmente processi di scambio ionico, simili alle reazioni chimiche in soluzione, tranne per il fatto che si verificano in mezzi eterogenei (solidi e liquidi). Prima e dopo la reazione, la struttura stessa della resina non cambia. Questo problema di "chi scambia chi" è essenzialmente un processo di reazione reversibile. Affinché lo scambio ionico proceda senza intoppi, l'equilibrio chimico deve essere interrotto, spingendo la reazione verso destra e rimuovendo quanto più possibile la sostanza appena formata dalla soluzione. Prendendo come esempio lo scambio tra resina di tipo RNa- e CaCl2, come mostrato nell'equazione seguente:
![]()
Secondo l'equilibrio chimico, la reazione statica nell'equazione precedente raggiunge uno stato di equilibrio dopo un certo punto, il che significa che non tutto il Na+ sulla resina RNa è stato scambiato. Per aumentare l'effetto addolcitore dell'acqua e spingere la reazione verso destra, il NaCl generato deve essere rimosso tempestivamente.
Sulla base di questo principio, nella pratica produttiva, la resina di tipo RNa- viene posta in uno scambiatore di ioni, consentendo all'acqua contenente CaCl2 di fluire continuamente attraverso di esso, rimuovendo così continuamente il NaCl generato. In questo modo, gli ioni Na+ sulla resina possono scambiarsi continuamente con gli ioni Ca2+ nell'acqua fino a quando non vengono scambiati quasi tutti gli ioni Na+ sulla resina. Questo è il principio base dello scambio ionico. Il processo di rigenerazione è l'opposto: gli ioni Na+ si scambiano con ioni Ca2+ sulla resina di tipo R2Ca- e il CaCl2 generato viene rimosso immediatamente, il che è vantaggioso per la rigenerazione.
II. Equilibrio e interruzione dello scambio ionico
La reazione reversibile di scambio ionico obbedisce alla "legge dell'azione di massa" e la costante di equilibrio K della reazione di scambio ionico può essere espressa dalla seguente formula:
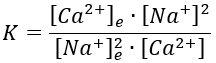
Dove: [Ca2+]e è la concentrazione di Ca2+ sulla resina all'equilibrio della reazione; [Na+]e è la concentrazione di Na+ sulla resina all'equilibrio della reazione; [Ca2+] è la concentrazione di Ca2+ nell'acqua all'equilibrio della reazione; [Na+]e è la concentrazione di Na+ nell'acqua all'equilibrio della reazione.
Il lato sinistro della formula sopra rappresenta il rapporto tra la concentrazione di Ca2+ e la concentrazione di Na+ all'interno della resina. Se questo valore è elevato indica che la concentrazione di Ca2+ è molto maggiore della concentrazione di Na+, e la resina è essenzialmente del tipo R2Ca; se questo valore è piccolo la resina è essenzialmente di tipo RNa. Il primo è il requisito per l'effetto ammorbidente, il secondo è il requisito per l'effetto rigenerante.
Come si può vedere dalla formula, la grandezza di [Ca2+]e/[Na+]e² dipende dalla costante di equilibrio K e dalla grandezza di [Ca2+]/[Na+]² nell'acqua. L’analisi di questi due fattori è la seguente:
(1) Il valore K è una costante maggiore di 1, riflettendo quindi la tendenza intrinseca di Ca2+ a sostituire Na+ tra i due ioni. Questa tendenza è determinata dal potenziale di scambio tra questi due ioni e la resina stessa, riflettendo la tendenza fondamentale di "chi scambia chi".
(2) Il fattore [Ca2+]/[Na+]2 riflette le concentrazioni relative di Ca2+ e Na+ nell'acqua. Questa relazione cambia con la qualità dell'acqua e può essere intervenuta artificialmente.
Quando si utilizza lo scambio ionico per addolcire l'acqua con bassa salinità, sia le concentrazioni di Ca2+ che di Na+ sono basse, ma la concentrazione di Ca2+ è relativamente molto più alta della concentrazione di Na+. Ciò si traduce in un valore [Ca2+]/[Na+]2 elevato. Poiché anche il valore K è maggiore di 1, il prodotto dei due è ancora maggiore, portando a un valore [Ca2+]e/[Na+]e2 elevato. Ciò riflette il fatto che dopo lo scambio ionico la resina è essenzialmente del tipo R2Ca. Quando si utilizza lo scambio ionico per addolcire le acque reflue ad alta-salinità, le concentrazioni di Ca²⁺ e Na⁺ nell'acqua sono molto elevate, mentre la concentrazione di Ca²⁺ è molto inferiore a quella di Na⁺. Ciò si traduce in un valore [Ca²⁺]/[Na⁺]² molto piccolo che, moltiplicato per il valore K, è anch'esso molto piccolo. Pertanto, è difficile ottenere un valore [Ca²⁺]e/[Na⁺]e² elevato, il che significa che la resina è difficile da convertire nella forma R₂Ca durante lo scambio ionico. Ciò riflette la difficoltà di utilizzare lo scambio ionico per ammorbidire le acque reflue ad alta-salinità.
Durante la rigenerazione, vogliamo che la resina sia completamente convertita nella forma RNa. Per rendere il valore [Ca²⁺]e/[Na⁺]e² molto piccolo, l'unico modo fattibile è aumentare la concentrazione di Na⁺ nell'acqua. Questo è il motivo per cui la concentrazione di sale durante la rigenerazione deve raggiungere il 6%~10%.
Per la rigenerazione della resina di tipo RH-, se si utilizza HCl come rigenerante, vengono prodotti CaCl₂ e MgCl₂. Entrambe queste sostanze hanno un'elevata solubilità in acqua, quindi non vi è alcun problema di precipitazione. Pertanto non esiste alcuna limitazione specifica alla concentrazione della soluzione di HCl. Tuttavia, quando si utilizza H2SO4 come rigeneratore, la solubilità del CaSO4 risultante (gesso) è molto bassa. Pertanto, è fondamentale prevenire la precipitazione di CaSO4. Le precipitazioni possono ostruire i pori della rete-reticolata della resina, facendo perdere alla resina parte della sua capacità di scambio. Pertanto, quando si utilizza H2SO4 come rigeneratore, la concentrazione dovrebbe essere limitata all’1%–2% e la velocità di rigenerazione non dovrebbe essere troppo bassa.
In sintesi, lo scambio ionico non è semplicemente un adsorbimento fisico, ma una reazione di scambio reversibile dominata dall’equilibrio chimico. Comprenderne l'essenza è essenziale per le applicazioni pratiche dell'ingegneria. Per i sistemi di addolcimento, padroneggiare la relazione tra la costante di equilibrio della reazione e la concentrazione di ioni nell'acqua è fondamentale per ottenere uno scambio efficiente e una rigenerazione economica. Per il trattamento delle acque reflue ad alta-salinità, è ancora più necessario superare i limiti di equilibrio modificando le condizioni operative o impiegando processi compositi. Che si tratti dell'approvvigionamento idrico industriale o del riutilizzo delle acque reflue industriali, la selezione razionale e il controllo della rigenerazione delle resine a scambio ionico sono fondamentali per il funzionamento stabile del sistema e il risparmio energetico. Solo combinando la teoria con l’esperienza sul campo è possibile realizzare veramente il valore fondamentale della tecnologia di scambio ionico nel moderno trattamento delle acque.
